La Materia
Llamamos materia a todo aquello que forma el universo, tiene masa y ocupa un lugar en el espacio, por lo tanto es mensurable y cuantificable (la podemos medir y contar). La materia está formada por átomos, que son partículas diminutas que se agrupan para formar objetos. Los átomos están formados por un núcleo, constituido por protones y neutrones alrededor del cual orbitan unas partículas más diminutas llamadas electrones, como si fuera un pequeño sistema solar.
Estados de agregación de la materia
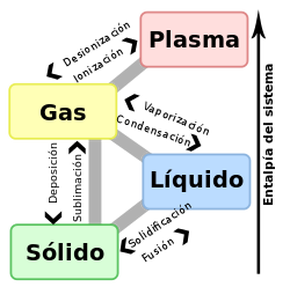
En la naturaleza podemos encontrar la materia en varios estados fundamentales, dependiendo cómo estén unidos sus átomos, así, sabemos que existen cuatro estados de la materia observables a simple vista, demos una descripción breve de cada uno de ellos:
Llamamos materia a todo aquello que forma el universo, tiene masa y ocupa un lugar en el espacio, por lo tanto es mensurable y cuantificable (la podemos medir y contar). La materia está formada por átomos, que son partículas diminutas que se agrupan para formar objetos. Los átomos están formados por un núcleo, constituido por protones y neutrones alrededor del cual orbitan unas partículas más diminutas llamadas electrones, como si fuera un pequeño sistema solar.
Estados de agregación de la materia
En la naturaleza podemos encontrar la materia en varios estados fundamentales, dependiendo cómo estén unidos sus átomos, así, sabemos que existen cuatro estados de la materia observables a simple vista, demos una descripción breve de cada uno de ellos:
- Sólido: los átomos están muy unidos, lo que permite que soporten fuerzas sin deformarse, por lo que podemos decir que tienen una forma definida y son incompresibles (no se pueden comprimir)
- Líquido: aquí los átomos están unidos entre sí, pero con menos fuerza, por lo que presenta una forma fluida, es decir, no tiene forma definida, siendo además poco o nada compresibles.
- Gaseoso: aquí los átomos están desligados unos de otros, esto implica no sólo que no tienen forma definida, sino que, además, ocupan todo el volumen posible, apartándose unos de otros hasta llenar todo el espacio. Esta cualidad puede invertirse, por lo que son elementos compresibles.
- Plásmico: es similar al gaseoso, con la diferencia de que las partículas han perdido un electrón. Este tipo de "gas" es capaz de conducir la electricidad, por lo que nos resulta muy útil, por ejemplo, para fabricar los tubos fluorescentes que iluminan el colegio.
Respecto a las Propiedades, podemos distinguir dos tipos de propiedades de la materia: Propiedades Físicas y Propiedades Químicas.
Propiedades Físicas de la materia.
Son aquellas que sólo dependen de la sustancia, sin interaccionar con otra sustancia.
Podemos diferenciar entre propiedades generales y propiedades específicas. Vamos a ver cada una de ellas.
Propiedades generales de la materia.
Las tienen en común todos los tipos de materia y son la MASA y el VOLUMEN.
Propiedades específicas de la materia.
Son aquellas que nos permiten diferenciar una materia de otra, como el color, la dureza, el brillo, el olor, la textura, la densidad... Vamos a hablar de ésta última.
Llamamos densidad al cociente entre la masa y el volumen de un objeto. Medimos la densidad en g/m3 con sus distintos múltiplos y submúltiplos. Cada sustancia tiene una densidad diferente, lo que nos permite distinguirla de otra, como hizo Arquímedes en la antigüedad (Arquímedes y la Corona).
Elementos, Compuestos y Mezclas
En la naturaleza encontramos la materia de diversas formas, puede ser el resultado de la combinación de varias sustancias o bien encontramos la sustancia pura.
Cuando encontramos este último caso, la sustancia pura, tal cual, estamos hablando de un Elemento. Ejemplos son el aluminio, el oro, el azufre... en los que toda la materia está formada por el mismo tipo de átomos.
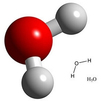
Cuando los átomos de distintos elementos se combinan entre sí forman los Compuestos. El agua es un buen ejemplo, ya que está formada por dos átomos de Hidrógeno y uno de Oxígeno:
Propiedades Físicas de la materia.
Son aquellas que sólo dependen de la sustancia, sin interaccionar con otra sustancia.
Podemos diferenciar entre propiedades generales y propiedades específicas. Vamos a ver cada una de ellas.
Propiedades generales de la materia.
Las tienen en común todos los tipos de materia y son la MASA y el VOLUMEN.
- Masa: es la cantidad de materia que posee un cuerpo. Esta cantidad de materia la medimos en gramos (g), con sus múltiplos (Kg, T...) y submúltiplos (dg, cg, mg...).
- Volumen: es el espacio que ocupa una cantidad de materia concreta y lo medimos en metros cúbicos o en litros, con sus múltiplos y submúltiplos.
Propiedades específicas de la materia.
Son aquellas que nos permiten diferenciar una materia de otra, como el color, la dureza, el brillo, el olor, la textura, la densidad... Vamos a hablar de ésta última.
Llamamos densidad al cociente entre la masa y el volumen de un objeto. Medimos la densidad en g/m3 con sus distintos múltiplos y submúltiplos. Cada sustancia tiene una densidad diferente, lo que nos permite distinguirla de otra, como hizo Arquímedes en la antigüedad (Arquímedes y la Corona).
Elementos, Compuestos y Mezclas
En la naturaleza encontramos la materia de diversas formas, puede ser el resultado de la combinación de varias sustancias o bien encontramos la sustancia pura.
Cuando encontramos este último caso, la sustancia pura, tal cual, estamos hablando de un Elemento. Ejemplos son el aluminio, el oro, el azufre... en los que toda la materia está formada por el mismo tipo de átomos.
Cuando los átomos de distintos elementos se combinan entre sí forman los Compuestos. El agua es un buen ejemplo, ya que está formada por dos átomos de Hidrógeno y uno de Oxígeno:
Hablamos de Mezclas cuando la combinación de elementos no se da a nivel molecular, sino que cada elemento sigue siendo independiente, pudiendo mezclarse sólo elementos simples, elementos con compuestos o varios compuestos entre sí. Aquí podemos hacer una nueva clasificación, ya que las mezclas pueden ser Homogéneas o Heterogéneas.
Además, las mezclas podemos separarlas con relativa facilidad, no así los compuestos. Hay diferentes técnicas para separar los componentes de una mezcla. Vamos a ver algunos:
Cambios en la materia: cambios físicos y cambios químicos.
Sabemos, porque lo vemos continuamente, que si cambiamos las condiciones de temperatura o presión, podemos inducir cambios en la materia, también podemos provocar cambios al combinar unos tipos de materia con otros. Así, concluimos que hay dos tipos de cambios en la materia: Cambios Físicos y Cambios Químicos.
Cambios Físicos de la materia
Son aquellos en los que no hay ningún cambio en la composición de la materia, por lo que las propiedades de esa materia no varían. En general, los cambios físicos son reversibles, por lo que podemos volver a obtener la sustancia con su forma original. Así, podemos citar los siguientes:
Cambios Químicos de la materia
Al contrario que en los cambios físicos, en los cambios químicos varía la composición y estructura de la materia, generando una sustancia (o más de una) nueva. Este cambio indica que, a nivel atómico, se han reordenado los electrones formando una sustancia distinta de la original. Este cambio atómico significa que las propiedades de la materia original han cambiado. Los cambios químicos son, en su mayoría, irreversibles, es decir, no podemos volver a la sustancia original (en algunos casos sí es posible, para lo que necesitamos volver a hacer un cambio químico a la nueva sustancia).
Los cambios químicos se denominan reacciones químicas, consistiendo en la combinación de sustancias, llamadas reactivos, para obtener una nueva sustancia (o varias) llamada producto.
Hemos visto ejemplos de esto con los experimentos de clase, como cuando mezclábamos bicarbonato sódico y vinagre, extracto de lombarda con vinagre o con bicarbonato, disoluciones de hierro con otros componentes...
Una reacción química muy común es la que mezcla oxígeno con otras sustancias, a esta reacción la llamamos oxidación.
Y ahora... lo que todo el mundo esperaba:
- Mezclas homogéneas son aquellas en las que la combinación de sustancias es uniforme, es decir, no distinguimos al final los distintos componentes, un claro ejemplo son las disoluciones, donde tenemos un disolvente y un soluto, como cuando preparamos leche con cacao (cada uno con sus propiedades), al remover no podemos distinguir a simple vista dónde está cada sustancia, sino que tenemos una mezcla uniforme con unas propiedades distintas a las de cada sustancia por separado.
- Mezclas heterogéneas son aquellas en las que la combinación de las sustancias no es uniforme, cada sustancia conserva sus propiedades; como cuando mezclamos agua y arena, por mucho que removamos la mezcla, siempre podremos diferenciar a simple vista el agua de los granos de arena y tanto el agua como la arena conserva sus propiedades intactas.
Además, las mezclas podemos separarlas con relativa facilidad, no así los compuestos. Hay diferentes técnicas para separar los componentes de una mezcla. Vamos a ver algunos:
- Decantación: la usamos cuando queremos separar componentes con distinta densidad. Para ello dejamos reposar un tiempo los componentes de la mezcla hasta que las distintas densidades hacen que se separen, yendo los menos densos hacia arriba y los más densos al fondo del recipiente.
- Filtración: con este sistema separamos un componente sólido de uno líquido, para ello usamos filtros de distintos grosores.
- Evaporación: aplicamos calor a la mezcla hasta que separamos el disolvente del soluto.
- Magnetismo: cuando queremos separar una mezcla con componentes magnéticos de otros que no lo son.
Cambios en la materia: cambios físicos y cambios químicos.
Sabemos, porque lo vemos continuamente, que si cambiamos las condiciones de temperatura o presión, podemos inducir cambios en la materia, también podemos provocar cambios al combinar unos tipos de materia con otros. Así, concluimos que hay dos tipos de cambios en la materia: Cambios Físicos y Cambios Químicos.
Cambios Físicos de la materia
Son aquellos en los que no hay ningún cambio en la composición de la materia, por lo que las propiedades de esa materia no varían. En general, los cambios físicos son reversibles, por lo que podemos volver a obtener la sustancia con su forma original. Así, podemos citar los siguientes:
- Cambios de estado: fusión, evaporación, sublimación, ionización... (ver esquema de arriba)
- Deformación: cambiamos su forma al aplicar una fuerza de presión sobre la materia.
- Dilatación: al aumentar su volumen por cambios en la temperatura, pero no tanto como para provocar un cambio de estado.
- Contracción: disminuimos el volumen de la materia variando su temperatura, pero no tanto como para provocar un cambio de estado.
Cambios Químicos de la materia
Al contrario que en los cambios físicos, en los cambios químicos varía la composición y estructura de la materia, generando una sustancia (o más de una) nueva. Este cambio indica que, a nivel atómico, se han reordenado los electrones formando una sustancia distinta de la original. Este cambio atómico significa que las propiedades de la materia original han cambiado. Los cambios químicos son, en su mayoría, irreversibles, es decir, no podemos volver a la sustancia original (en algunos casos sí es posible, para lo que necesitamos volver a hacer un cambio químico a la nueva sustancia).
Los cambios químicos se denominan reacciones químicas, consistiendo en la combinación de sustancias, llamadas reactivos, para obtener una nueva sustancia (o varias) llamada producto.
Hemos visto ejemplos de esto con los experimentos de clase, como cuando mezclábamos bicarbonato sódico y vinagre, extracto de lombarda con vinagre o con bicarbonato, disoluciones de hierro con otros componentes...
Una reacción química muy común es la que mezcla oxígeno con otras sustancias, a esta reacción la llamamos oxidación.
Y ahora... lo que todo el mundo esperaba:
¡¡LOS VÍDEOS DE LOS EXPERIMENTOS!!
Ha
sido una experiencia muy instructiva y divertida. Estoy muy orgulloso
de todos los que habéis trabajado en vuestro experimento, cómo lo habéis
presentado y cómo lo habéis ejecutado.
Ah, tened paciencia con los que faltan, que esto tarda mucho en subirse...
Ah, tened paciencia con los que faltan, que esto tarda mucho en subirse...
|
|
|
|
|
|
|
|
|
|
|
|
|
|